Caterina Lanna
UO di Dermatologia. Policlinico Universitario di Roma Tor Vergata
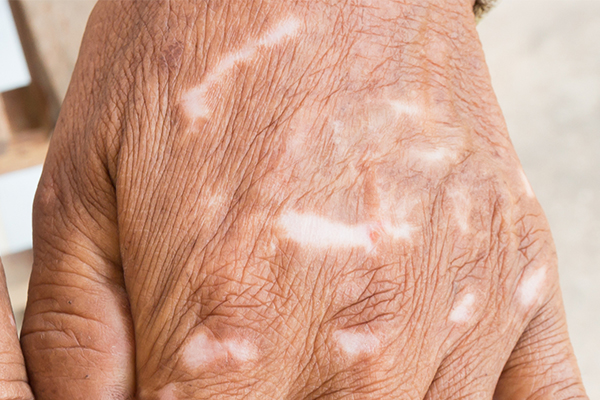
La sclerodermia è una rara malattia del tessuto connettivo che si manifesta con sclerosi cutanea e coinvolgimento sistemico variabile. Sono note due categorie di sclerodermia:
- sclerosi sistemica, caratterizzata da sclerosi cutanea e coinvolgimento viscerale
- sclerodermia localizzata o morfea, classicamente benigna, ad evoluzione auto-limitata, confinata alla pelle e / o ai tessuti sottostanti.
Quest’ultima è a sua volta suddivisa in lineare, a placca, profonda, bollosa e generalizzata (1).
Si tratta di una patologia multifattoriale in cui al mosaicismo genetico si associano un processo infiammatorio e un probabile substrato autoimmunitario.
La sclerodermia non sembra essere una malattia esclusivamente cutanea. Quando viene diagnosticata, infatti, è necessario prestare particolare attenzione al coinvolgimento degli organi interni e all’associazione con altre malattie del tessuto connettivo (2).
La gestione terapeutica della morfea è ancora insoddisfacente, nonostante diverse modalità terapeutiche siano state suggerite, incluso l’uso di farmaci topici, immunosoppressori, terapie fisiche e fototerapia (2).
Mentre, infatti, alcuni pazienti rispondono bene all’uso di steroidi, sia topici che intralesionali, antimalarici o immunosoppressori tradizionali, esiste una percentuale significativa di pazienti che non rispondono a questi trattamenti o che ne richiedono alti dosaggi. Per questo gruppo di pazienti esiste dunque un’elevata necessità di trovare terapie alternative(3). Il Sarilumab, anticorpo monoclonale anti-IL-6, approvato per l’artrite reumatoide grave (AR) sembrerebbe rappresentare una nuova valida opportunità terapeutica per la morfea, visto il suo buon profilo di sicurezza nella AR e il ruolo dell’IL-6 nella patogenesi di tale patologia (4). L’IL-6 infatti risulterebbe aumentata nel siero dei pazienti affetti da morfea e inoltre l’inibizione di tale citochina avrebbe ottenuto ottimi risultati nel modello murino bleomicina-indotto di sclerosi cutanea, impedendo lo sviluppo della stessa fibrosi cutanea. Un altro promettente farmaco per la morfea è costituito dal composto FCX-013 e veledimex. Il primo componente, FCX-013, è costituito da fibroblasti umani autologhi geneticamente modificati mediante lentivirus, codificanti la metalloproteinasi 1 (MMP-1), una proteina responsabile della decomposizione del collagene. FCX-013 è progettato per essere iniettato sotto la pelle nella posizione delle lesioni fibrotiche in cui le cellule di fibroblasti geneticamente modificate produrranno MMP-1 per abbattere l’accumulo di collagene in eccesso. Il composto orale Veledimex, invece, è in grado di indurre l’espressione della proteina MMP-1 dalle cellule iniettate, normalizzando dunque la produzione di collagene in sede (5).Infine, il crisaborolo, inibitore della fosfodiesterasi-4, già approvato dalla FDA e in fase di approvazione in Europa per il trattamento della dermatite atopica, si sta rivelando un ottimo topico anche per il trattamento della morfea(6).
Bibliografia
-
- Tratenberg M, Gutwein F, Rao V, Sperber K, Wasserrman A, Ash J. Localized Scleroderma: A Clinical Review. Curr Rheumatol Rev. 2017;13(2):86–92.
- Bielsa Marsol I. Update on the classification and treatment of localized scleroderma. Actas Dermosifiliogr. 2013 Oct;104(8):654–66.
- Careta MF, Romiti R. Localized scleroderma: clinical spectrum and therapeutic update. An Bras Dermatol. 2015;90(1):62–73.
- Study to Assess Sarilumab in Halting Progression of Morphea – Full Text View – ClinicalTrials.gov [Internet]. [cited 2019 Sep 30]. Available from: https://clinicaltrials.gov/ct2/show/NCT03679845
- A Study of FCX-013 Plus Veledimex for the Treatment of Moderate to Severe Localized Scleroderma – Full Text View – ClinicalTrials.gov [Internet]. [cited 2019 Sep 30]. Available from: https://clinicaltrials.gov/ct2/show/NCT03740724
- Pilot Study Evaluating the Efficacy of a Topical PDE4 Inhibitor for Morphea – Full Text View – ClinicalTrials.gov [Internet]. [cited 2019 Sep 30]. Available from: https://clinicaltrials.gov/ct2/show/NCT03351114